
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

间变性淋巴瘤激酶(ALK)是非小细胞肺癌(NSCLC)重要的致癌驱动因子之一,研究表明,ALK激活之后能够导致下游信号通路被激活,进而引发肿瘤的发生和存活。据统计,中国每年约有2-7万人罹患ALK阳性肺癌,占肺癌病人的3%-11%。ALK基因突变被称为“钻石基因突变”,因为靶向药对ALK阳性肺癌疗效非常好。
据了解,目前获批治疗ALK阳性肺癌的靶向药:一代ALK靶向药:克唑替尼(国内已上市);二代ALK靶向药:阿来替尼(国内已上市)、色瑞替尼(国内已上市)、布加替尼(国内未上市);三代ALK靶向药:劳拉替尼(国内未上市)。
其中,克唑替尼一般在使用10-11月后出现耐药,且其血脑屏障透过率低,无法有效抑制肿瘤细胞的脑转移。CT-707是首药控股自主研发、具有完全知识产权的一类创新药,是全新结构的二代ALK抑制剂,初步研究结果表明,CT-707治疗克唑替尼耐药或者不耐受的患者,其疗效安全性可控。
随着国产二代ALK靶向药崛起,为ALK阳性肺癌患者带来了新的生存希望。目前,首药控股申办的“评价CT-707治疗克唑替尼耐药晚期ALK阳性非小细胞肺癌患者有效性及安全性的Ⅱ期临床研究”在全国多中心开展,获得良好的效果。
以下为河南省人民医院肿瘤内科的相关临床研究病例分析:
患者Z,女,33岁。2019年10月初因“咳嗽、胸闷、胸痛”就诊,CT(2019-10-10)显示:
1.结合病史考虑右肺下叶肺癌;
2.右肺门及纵隔内淋巴结转移;3.肝脏异常密度影,转移可能。脑平扫+增强核磁显示:小脑蚓部及左侧小脑半球、双侧枕叶异常信号,考虑脑转移。肺穿刺活检病理显示:肺腺癌。基因检测:EGFR 基因未检测到突变,ALK-D5F3(弥漫强+),ROS1 野生型。于2019年10月12日开始口服克唑替尼靶向治疗。1 个月后(2019-11-11)复查 CT 显示:1.“右肺癌靶向治疗后”改变,较2019-10-09 相仿;2.右侧颈根部、锁骨下区、右肺门及纵隔内淋巴结转移;
3.肝脏异常密度影,较2019-10-09增多。医生判定为疾病进展, 停用克唑替尼治疗。
患者在河南省人民医院就诊,经医生评估后符合二代ALK抑制剂 CT-707的新药临床试验入组条件,于2019年11月29日开始口服 CT-707,经2周期(21天/周期)治疗后复查 CT,肺内靶病灶完全消失,肝内靶病灶肿瘤缩小55%,咳嗽、胸闷、胸痛等症状明显减轻。2020年10月26日,经治疗16周期后复查,患者肺内、肝内靶病灶达到完全缓解。截至目前,患者口服CT-707 治疗18周期,期间仅出现1级血清天门冬氨酸氨基转移酶(AST)升高及1级腹泻,其他未见严重不良反应。
以下为克唑替尼治疗前(2019-10-10)、治疗1月后(2019-11-11)靶病灶部分影像。
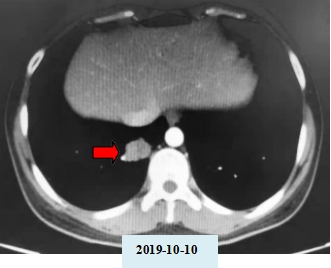
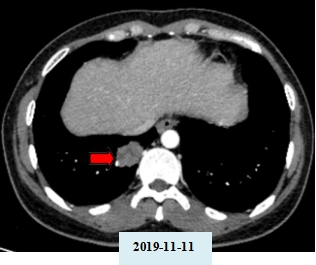
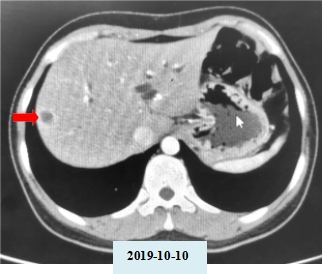
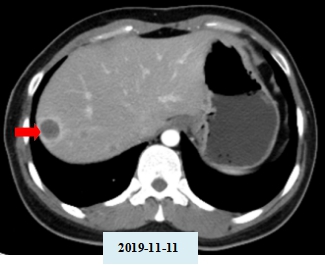
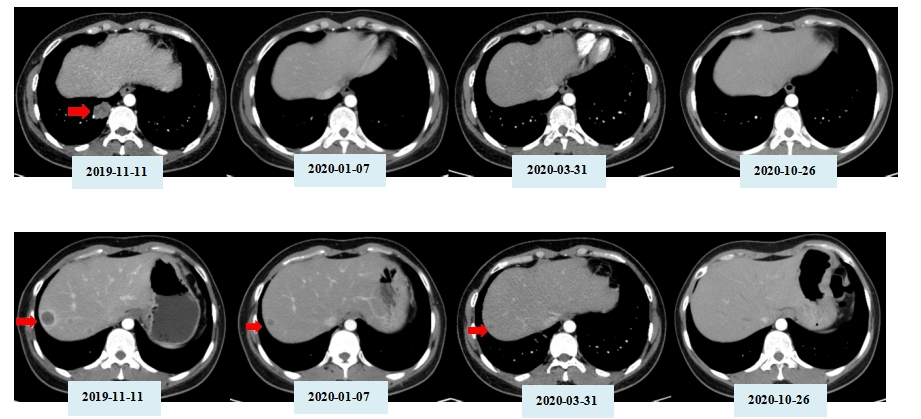
以下为CT-707治疗前(2019-11-11)、治疗 2 周期(2020-01-07)、治疗6周期(2020-3-31)、治疗 16 周期(2020-10-26)靶病灶部分影像资料。
CT-707为高活性的ALK/FAK/Pyk2/IGF-1R抑制剂,用于治疗晚期恶性肿瘤,是首药控股自主研发的1类新药。目前,除了正在进行的Ⅱ期临床研究外,CT-707同时还在全国多家医院开展“比较CT-707 与克唑替尼治疗ALK阳性晚期非小细胞肺癌患者有效性和安全性的多中心、随机、开放Ⅲ期临床研究”。
资料显示,首药控股(北京)股份有限公司成立于2016年,是由市、区两级政府共同参股的混合所有制企业。公司总部位于北京经济技术开发区,专注于肿瘤和糖尿病创新药的研发和生产。秉持“创好药、造中国患者能够吃得起的一类新药”理念,首药控股已获发明专利授权逾百项,国家一类新药临床批件16个(包括合作研发项目),荣获国家“十二五”“十三五”重大新药创制专项9项。其中,已有2个新药进入临床III期、2个新药进入临床II期、9个新药进入临床I期,涵盖肺癌、乳腺癌、肝癌、淋巴瘤、胰腺癌等癌种。
(河南省人民医院肿瘤内科 卢创新副主任医师 仓顺东主任医师 )
